廈門外泌體提取試劑廠家
外泌體的提取、分離方法:梯度密度離心法。研究發現,外泌體的密度在1.1~1.19kg·L-1之間,因此,可以采用密度梯度離心法來分離外泌體。該方法是將超速離心結合蔗糖密度梯度或蔗糖墊結合,原理是先除去非囊泡物質,再通過梯度密度濃縮提取外泌體,該方法可以得到相對較為純凈的外泌體。傳統的梯度密度方法通常需要離心16h,但是2012年,研究者[15]使用了62~90h才分離出某些確切囊泡,因此,該方法可能不足以沉淀所有的外泌體。如果離心時間不充足,污染物質可能和外泌體保持在相同的密度層,特別是這個密度范圍又比較寬。活細胞分泌到胞外的囊泡樣小體,含有多種蛋白和核酸分子(DNA、RNA、以及miRNA)。廈門外泌體提取試劑廠家

外泌體與免疫系統:不同的細胞來源的外泌體,包括免疫細胞(B細胞和樹突狀細胞)、病細胞、上皮細胞和間充質細胞,釋放出帶有載體的外泌體,可影響先天免疫系統和適應性免疫系統中受體細胞的增殖和各自的活性。CD4+和CD8+T細胞可直接或間接地受到外泌體的影響,刺激或壓制其增殖和功能。外泌體與代謝性和心血管疾病:外泌體可以通過攜帶miRNA或代謝物分子在代謝性疾病和心血管疾病的發生的發展過程中起作用。體外培養心血管疾病的細胞收集的外泌體與疾病相關的代謝適應有關;體外培養的間充質干細胞和胚胎干細胞的外泌體具有保護心血管的作用。這些發現表明不同來源的外泌體可以通過傳遞miRNA,蛋白等物質改變受體細胞的代謝狀態。外泌體檢測作為一種新型的液體活檢熱點技術已被許多臨床科研機構普遍地應用于一些病癥和疾病的無創診斷廈門正規外泌體提取試劑服務電話外泌體攜帶大量特異性的蛋白質以及功能性的mRNAs、miRNAs等生物活性物質。

研究初次發現瘧原蟲傳染小鼠血漿外泌體(exosomes)能夠壓制一些病癥血管生成,并初步闡明其分子機制。研究加深了對瘧原蟲傳染宿主所分泌的外泌體與一些病癥血管生成之間的相互作用的認識,為開發瘧原蟲傳染來源的外泌體作為一種新型抗一些病癥制劑奠定了基礎。研究人員選用肺病小鼠模型作為研究對象,從傳染瘧原蟲的小鼠血漿中獲得外泌體,并將這些外泌體注射到小鼠的一些病癥內部,并與沒有瘧原蟲傳染的小鼠血漿外泌體進行對照。研究發現,瘧原蟲傳染小鼠的血漿外泌體明顯壓制一些病癥血管的生成。進一步的研究發現,瘧原蟲傳染的小鼠血漿外泌體通過至少四種特殊的微小RNA(miR16-5p/17-5p/322-5p/497-5p)壓制血管內皮細胞VEGF受體(VEGFR2)的表達從而阻斷血管生成的信號通路。這些發現加深了人們對瘧原蟲抗病機理的理解,并為瘧原蟲療法治病一些疾病的臨床研究提供進一步的理論依據。
外泌體的提取主要包括以下幾種方式。一是超速離心法,這是目前外泌體提取較常用的方法。此種方法得到的外泌體量多,但是純度不足,電鏡鑒定時發現外泌體聚集成塊,由于微泡和外泌體沒有非常統一的鑒定標準,也有一些研究認為此種方法得到的是微泡不是外泌體。二是過濾離心,這種操作簡單、省時,不影響外泌體的生物活性,但同樣存在純度不足的問題。三是密度梯度離心法,用此種方法分離到的外泌體純度高,但是前期準備工作繁雜,耗時,量少。、外泌體提取:磁珠法具有特異性高、操作簡便、不影響外泌體形態完整等優點。
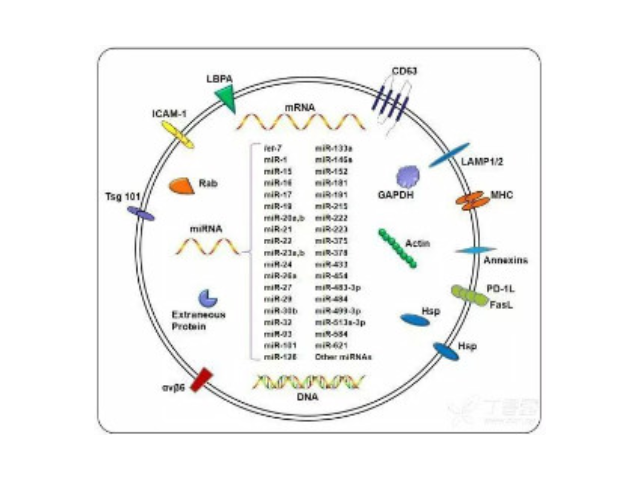
外泌體(exosomes,Exos)是細胞分泌的一種膜囊泡,因其可以將供體細胞的信息通過其攜帶的蛋白質、mRNA、miRNA等傳遞到受體細胞,實現細胞之間的信息交流及物質交換,并且可以作為藥物載體轉運藥物而引起科學家的普遍關注(Fig1)。外泌體作為內源性的天然藥物載體有著獨特的優勢,表面由脂質和蛋白質組成,使其可以穿透許多生物膜,提高藥物的運輸效率和靶向性,可以穩定存在于血液中,納米級尺寸明顯增強藥物在瘤部位的滲透滯留效應(permeabilityandretentioneffect,EPR)。目前,許多抗藥物、基因藥物及藥物均被成功載入外泌體。但是由于沒有較好的外泌體分離純化和載藥的方法,使得其作為藥物載體的應用受到限制。外泌體提取:樣本的粘度與分離的外泌體純度有顯著的相關性。杭州正規外泌體提取試劑哪里買
超濾離心法簡單高效,且不影響外泌體的生物活性,但同樣存在純度不高的問題。廈門外泌體提取試劑廠家
外泌體的提取主要包括以下幾種方式。一是超速離心法,這是目前外泌體提取較常用的方法。此種方法得到的外泌體量多,但是純度不足,電鏡鑒定時發現外泌體聚集成塊,由于微泡和外泌體沒有非常統一的鑒定標準,也有一些研究認為此種方法得到的是微泡不是外泌體。二是過濾離心,這種操作簡單、省時,不影響外泌體的生物活性,但同樣存在純度不足的問題。三是密度梯度離心法,用此種方法分離到的外泌體純度高,但是前期準備工作繁雜,耗時,量少。外泌體檢測作為一種新型的液體活檢熱點技術已被許多臨床科研機構普遍地應用于一些病癥和疾病的無創診斷。廈門外泌體提取試劑廠家
- 唐山正規外泌體提取試劑單價 2025-06-15
- 成都正規外泌體提取試劑 2025-06-15
- 唐山外泌體提取試劑廠家供應 2025-06-15
- 深圳外泌體提取試劑供應商 2025-06-15
- 杭州正規外泌體提取試劑廠家供應 2025-06-15
- 武漢正規外泌體提取試劑推薦廠家 2025-06-15
- 溫州正規外泌體提取試劑廠家現貨 2025-06-14
- 南京正規外泌體提取試劑服務電話 2025-06-14
- 寧波外泌體提取試劑服務電話 2025-06-14
- 太原外泌體提取試劑廠家供應 2025-06-14
- 江門處理介質水性清洗劑供應商 2025-06-15
- 江蘇高性能聚氨酯膠冷鏈運輸 2025-06-15
- 廣東化學**市場價 2025-06-15
- 杭州鋼結構防腐涂料商家 2025-06-15
- 浙江本地防腐涂料廠家電話 2025-06-15
- 鹽城天然乳化劑價格 2025-06-15
- 廣東多功能應變測量儀器商家 2025-06-15
- 沈陽車輛應力應變測量儀廠家 2025-06-15
- 蘇州環保無味1B73 2025-06-15
- 智能全密閉溶劑型清洗機定制廠家推薦訂購 2025-06-15